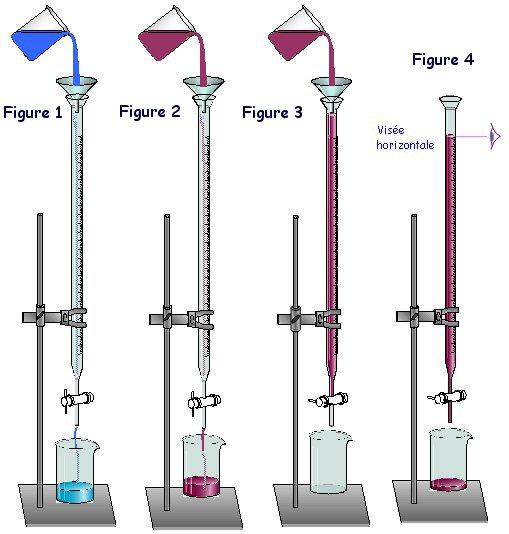
cromatografía
 |
| tomado de:(alvarez,2016) |
La Cromatografía es una técnica de separación en la que los componentes de una muestra se separan en dos fases: una fase estacionaria de gran área superficial, y una fase móvil. El objetivo de la fase estacionaria es retrasar el paso de los componentes de la muestra. Cuando los componentes pasan a través del sistema a diferentes velocidades, estos se separan en determinados tiempos. Cada componente tiene un tiempo de paso característico a través del sistema, llamado tiempo de retención. La separación cromatográfica se logra cuando el tiempo de retención del analito difiere del resto de componentes de la muestra.
La cromatografía es una de los principales métodos analíticos y permite la separación y cuantificación de sustancias muy similar en estructura y propiedades químicas.
Clasificación de la técnica de cromatografía:
Cromatografía plana
Se realiza sobre papel u otro material sólido. Suele llamarse “en capa fina” o “en capa delgada” porque la fase estacionaria recubre un soporte plano y rígido.
Cromatografía de gases
Con fase móvil gaseosa.
- Cromatografía gas-líquido
- Cromatografía gas-sólido
Cromatografía líquida
Con fase móvil líquida.
- Cromatografía líquido-líquido
- Cromatografía líquido-sólido
Cromatografía de adsorción
(atención: es adsorción, no absorción)
Diferente afinidad de adsorción de los componentes de la muestra sobre la superficie de un sólido activo. La adsorción es la capacidad de las superficies para fijar moléculas.
La F.E. es siempre sólida. Ejemplos: alúmina, gel de sílice, carbón activo, fosfato cálcico, hidroxiapatito.
Cromatografía de reparto
Diferente solubilidad de los componentes de la muestra en la fase estacionaria (caso de la cromatografía de gases), o diferentes solubilidades de los componentes en las fases móvil y estacionaria (caso de la cromatografía líquida).
Ejemplos: en cromatografía plana, la F.E. es el agua o disolvente asociados a la celulosa (papel) o al soporte sólido que forma la capa fina; en columna, como F.E. se usan tierra de diatomeas, gel de sílice, celulosa en polvo...
Cromatografía de intercambio iónico
Diferente afinidad de los componentes de la muestra para el intercambio de iones. ¿Qué significa intercambio de iones? La F.E. posee carga eléctrica y por ello interacciona con los componentes de la muestra que tienen carga opuesta.
- Intercambio aniónico: F.E. con carga positiva, une aniones, bien los del disolvente (F.M.) o bien los de la muestra (de ahí la palabra intercambio).
- Intercambio catiónico: F.E. con carga negativa, une cationes, bien los del disolvente (F.M.) o bien los de la muestra.
usos y aplicaciones en la industria:
En la industria del petróleo juega una función primordial, por medio de la cromatografía se pueden analizar los constituyentes de las gasolinas, las mezclas de gases de refinería, gases de combustión, etc.
 |
| tomado de:(Pérez,2016) |
fabrica de cosméticos: control de calidad de producto, por ejemplo, porcentaje de esmalte de uñas,colorantes en casi todos los productos elaborados,porcentaje de control,en las esencias que se utilizan para la confección de perfumes,etc
 |
| tomado de:(roldan,2012) |
productos agroquímicos: determinación de concentración y porcentaje de solvente en un producto agroquímico terminado.
 |
| tomado de:(pregón agropecuario,2011) |
fuentes:
Laboratorio químico., (2014),
que es la cromatografía, recuperado de: https://www.tplaboratorioquimico.com/laboratorio-quimico/procedimientos-basicos-de-laboratorio/que-es-la-cromatografia.html,
7/11/2017
biomodel., (2013),
cromatografía, tomado de: http://biomodel.uah.es/tecnicas/crom/inicio.htm,
7/11/2017
quiminet., (2012), la cromatografía de gases
en la industria, recuperado de: https://www.quiminet.com/articulos/la-cromatografia-de-gases-en-la-industria-2876007.htm,
7/11/2017
Rodríguez, E., (2015), cromatografía,
recuperado de: https://es.slideshare.net/KiqueGTR/cromatografia-49074465,
7/11/2017